Вступление
Гиперосмолярная кома (ГОК) – это острая метаболическая декомпенсация сахарного диабета, характеризующаяся резко выраженными гипергликемией и дегидратацией, высокой осмолярностью плазмы, а также отсутствием кетоза и ацидоза. ГОК была впервые подробно охарактеризована в 1957 г. (Sament, Schwartz). Она встречается примерно в 6–10 раз реже, чем диабетический кетоацидоз (ДКА). При позднем начале лечения летальность при ГОК выше, чем при ДКА, и достигает 58–60%. По последним данным, частота ГОК – 5–15 % от всех острых гипергликемических состояний. У взрослых встречается с частотой 17,5 случаев на 100 000 населения в год. Преобладает ГОК у больных пожилого возраста с ИНСД, при этом она нередко является толчком к диагнозу (манифестационная кома). Однако в последние годы ГОК наблюдается не только при ИНСД, но и при инсулинзависимом сахарном диабете (ИЗСД) [7, 8, 13].
Предрасполагающие факторы
Пусковыми факторами развития ГОК служат состояния, характеризующиеся обезвоживанием и инсулиновой недостаточностью: инфекционные заболевания, особенно с высокой лихорадкой; рвота; диарея; неотложные состояния, такие как инфаркт миокарда, тромбоэмболия легочной артерии (ТЭЛА), острый панкреатит, кишечная непроходимость, мезентериальный тромбоз, инсульт, массивные кровотечения, обширные ожоги; почечная недостаточность; некоторые эндокринопатии (акромегалия, тиреотоксикоз, синдром Кушинга, несахарный диабет); травмы и физические воздействия — например, тепловой удар или переохлаждение [4, 8, 9] .
ГОК может возникнуть при приеме больших доз некоторых лекарственных средств: β-адреноблокаторов, блокаторов кальциевых каналов, диуретиков (фуросемида, маннитола, тиазидных диуретиков), диазоксида, циметидина, хлорпромазина, L-аспарагиназы, иммуносупрессоров, фенитоина, аналогов соматостатина, симпатомиметиков и особенно стероидов. Большинство этих препаратов являются дегидратирующими агентами или вызывают побочные реакции, а именно: нарушают высвобождение инсулина из поджелудочной железы или влияют на периферические эффекты инсулина. В генезе этого варианта комы играют особую роль хирургические методы детоксикации – гемодиализ, плазмаферез, перитонеальный диализ. Немалое значение имеют неправильные медицинские рекомендации по ограничению потребления жидкости при жажде, а также избыточное употребление углеводов внутрь или внутривенное введение большого количества глюкозы [2, 8].
Осмолярность плазмы крови
Осмолярность плазмы (P) представляет собой общее количество находящихся в плазменной воде твердых веществ, выраженное в мосм на 1 л воды. Эффективную осмолярность плазмы крови предлагается рассчитывать по упрощенной формуле: P (мосм) = 2[Na + K (ммоль/л)] + глюкоза крови (ммоль/л) + мочевина (ммоль/л) + белки (г/л) * 0,243/8. Нормальными считаются значения 297±2 мосм/л. Для ГОК осмолярность плазмы крови превышает 340 – 350 мОсм/л [7].
Основным осмотически активным катионом плазмы крови является натрий, осмолярность плазмы изменяется параллельно его концентрации. Норма концентрации натрия – 135 – 145 ммоль/л. Существует тесная связь между уровнем натрия и объемом циркулирующей крови. Так, увеличение концентрации натрия на 3 ммоль/л свыше 145 является показателем потери 1 л воды, концентрация натрия выше 160 ммоль/л свидетельствует о водном истощении организма. Нормальная концентрация калия во внеклеточной жидкости – 3,6 – 3 ммоль/л. Гиперкалиемией считается уровень калия более 5,5 ммоль/л. Концентрация глюкозы в крови может колебаться от 33,3 до 200 ммоль/л. Однако имеются указания на случаи развития гиперосмолярной комы при более низкой концентрации глюкозы в крови. Помимо указанных в формуле веществ, довольно значительной осмотической активностью обладают лактат, пируват, хлориды, среднетоксические молекулы при повышении их уровня. Поэтому, наряду с подсчетом, рекомендуется непосредственно определять осмолярность крови с помощью методов лабораторной диагностики [7].
Патогенез
Повышение уровня глюкозы, как и у пациентов с ДКА, является результатом сниженной утилизацией ее печенью, мышцами и жировой тканью, а также усиленной продукции глюкозы печенью. Относительный дефицит инсулина приводит к существенному повышению концентрации в крови антагониста инсулина – гормона глюкагона. Поскольку инсулин больше не сдерживает процессы, которые глюкагон стимулирует в печени, продукция глюкозы печенью резко усиливается. Продукция глюкозы при ГОК не превышает таковую при ДКА. [12]
Высокая осмолярность плазмы и дегидратация при ГОК развиваются вследствие длительного осмотического диуреза и недостаточного приема жидкости пациентом: как правило, больные старческого возраста не замечают постепенно нарастающее обезвоживание, поскольку ощущение жажды у них снижено. Потеря жидкости при ГОК составляет 8—12 л. [2]
У пациентов с сохранной функцией почек гипергликемия индуцирует осмотический диурез, который продолжается до тех пор, пока не снижается клубочковая фильтрация, вследствие дегидратации и, следовательно, гипоперфузии почек. Таким образом, осмотический диурез является основной причиной клеточной дегидратации (церебральной и экстрацеребральной). Ввиду продолжительного осмотического диуреза, элиминация глюкозы снижается или прекращается, в то время как продукция глюкозы печенью остается прежней. В результате – уровень гликемии возрастает. [12]
Существует гипотеза феномена умеренной выраженности дефицита инсулина при ГОК, обусловленного остаточной секрецией инсулина, достаточной для предотвращения активного липолиза и кетогенеза, но недостаточной для нормальной утилизации глюкозы жировой и мышечной тканью и подавления роста гликемии. Ранние теории объясняли это гиперосмолярностью и более низким уровнем свободных жирных кислот (СЖК), чем наблюдается при кетоацидотической коме. Экспериментально было подтверждено, что гиперосмолярность плазмы может устранять кетогенез путем подавления высвобождения СЖК из жировой такни, а низкий уровень свободных жирных кислот в плазме может снизить кетогенез ввиду отсутствия субстрата. Однако оба объяснения неубедительны, т.к. некоторые пациенты с ДКА имели осмолярнось плазмы выше, чем больные с гиперосмолярной комой, а гиперосмолярная кома возникала у пациентов с высоким уровнем СЖК в плазме [12].
Согласно другой гипотезе, при ГОК эндогенный инсулин в небольшом количестве попадает в печень, в то время как на периферии, в условиях более выраженной инсулиновой недостаточности, усиливается липолиз. Образующиеся в результате СЖК поступают в печень, где при наличии инсулина они являются субстратом для глюконеогенеза, но не превращаются в кетоновые тела. Возможны и другие объяснения отсутствия кетоза в условиях гипергликемии: иные соотношения инсулина и глюкагона, меньшие концентрации контринсулярных гормонов – соматотропного гормона (СТГ) и кортизола, однако подтвержденным можно считать лишь более низкий, чем при кетоацидозе, уровень СТГ. СТГ в физиологических дозах индуцирует липолиз и увеличивает концентрации СЖК и кетоновых тел в крови, следовательно, его более низкие концентрации при ГОК могут отчасти объяснять отсутствие кетоза [8].
Кроме того, гиперосмолярность угнетает высвобождение инсулина из поджелудочной железы в ответ на гипергликемию [2].
На основании исследований, проведенных на животных, было выявлено, что первопричиной отсутствия кетоацидоза является невосприимчивость печени к глюкагону, поэтому уровень малонил-КоА не снижается. У мышей линии ob/ob образование цАМФ глюкагоном заметно нарушается – концентрация малонил-КоА высокая. Причина невосприимчивости к глюкагону неясна, но у данных животных обнаружен дефект в аденилатциклазной системе, по крайней мере, в жировой ткани. Очевидно, что мыши линии ob/ob неравнозначны пациентам с инсулиннезависимым сахарным диабетом. Важно отметить, что невосприимчивость печени к глюкагону может тормозить кетоацидоз, но не оказывает никакого эффекта на гиперпродукцию глюкозы. Возможно, уровень малонил-КоА находится на ингибиторном уровне не по причине невосприимчивости печени к глюкагону, а из-за повышенного поглощения лактата печенью. Таким образом, увеличенный оборот лактата (цикл Кори) может быть следствием высокого содержания глюкозы в плазме. Увеличенное поглощение лактата и аланина достаточно для поддержания глюконеогенеза в печени с одновременным подавлением кетогенеза путем продукции малонил-КоА [12].
Гипернатриемия при ГОК обусловлена компенсаторной гиперпродукцией альдостерона в ответ на дегидратацию, при этом, в отличие от ДКА, натрий не выводится вместе с кетоновыми телами. Содержание натрия повышается и в спинномозговой жидкости (СМЖ), которая должна находиться в осмотическом равновесии с плазмой в условиях гипергликемии [8].
Последствием осмотического диуреза является также истощение общего калия. Дистальные канальцы максимально стимулируются альдостероном, и некоторое количество натрия реабсорбируется в обмен на калий. Ввиду большей длительности осмотического диуреза при ГОК потеря калия превышает таковую при ДКА и может достигать 400—1000 ммоль/л. Потеря калия может не повлечь клинических проявлений при правильном проведении регидратации. Во время осмотического диуреза происходит потеря и других ионов, таких как магний и фосфаты [3].
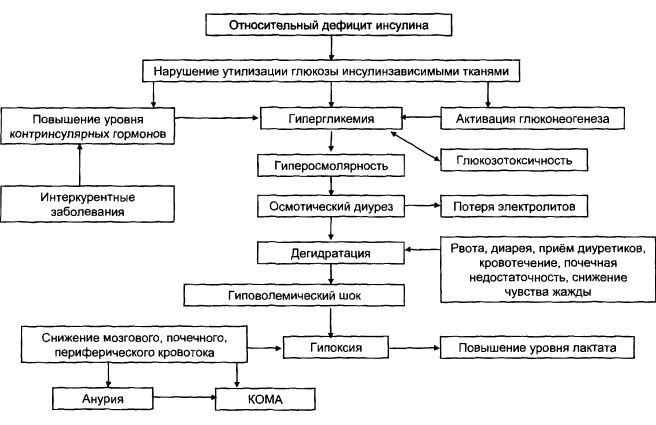
Рис. 1. Причины, механизмы и проявления диабетической гиперосмолярной комы [6].
Лабораторные показатели
Диагноз обычно подтверждается при лабораторных исследованиях. Основными показателями при этом являются концентрация глюкозы в крови, уровень кетонов плазмы и ее осмолярность. Дополнительные исследования включают полный клинический анализ крови и определение уровня электролитов, содержания азота мочевины в крови, креатинина и артериальных газов. Уровень электролитов плазмы может варьировать. Концентрация натрия колеблется от 120 до 160 ммоль/л, но, вследствие осмотического диуреза, больной почти всегда бывает гипертоничным, т.к. потери жидкости происходят без потерь натрия. Нужно учитывать, что при каждом повышении уровня глюкозы крови на 100 мг/дл уровень натрия снижается на 1,6ммоль/л. Такая гипонатриемия чаще всего является дилюционной и возникает в результате выхода свободной воды из клеток во внеклеточное пространство вследствие высокой осмолярности плазмы. В связи с этим необходимо рассчитывать истинную (скорректированную) концентрацию сывороточного натрия во избежание ошибок [3,5].
Расчет скорректированной концентрации натрия (cNA+) проводится по формуле:
сNa+ = Na+ пациента + 1,6 * (глюкоза крови пациента – 5,5)/5,5 [5].
Истощение запасов общего калия неизбежно и обычно бывает тяжелым. Потеря калия значительна ввиду большей продолжительности осмотического диуреза, а также из-за обильной рвоты, диареи и (иногда) применения калийуретических препаратов. Уровень азота мочевины почти всегда повышен из-за уменьшения экстрацеллюлярного объема и вследствие предшествующего заболевания почек. Начальный уровень азота мочевины, составляющий 3,3 – 5,0 ммоль/л, повышается пропорционально увеличению содержания креатинина в крови. Отношение азота мочевины к креатинину может составлять 30:1. По мере возмещения потерь жидкости азотемия разрешается, однако у 60—80 % больных концентрация азотистых шлаков в крови продолжает расти, вследствие хронического поражения почек [3].
Наличие метаболического ацидоза, обусловленного накоплением кетоновых тел, нехарактерно для ГОК, однако может иметь место ацидоз иного происхождения. По данным большинства исследований, 30—40 % больных имеют умеренно выраженный метаболический ацидоз, связанный с накоплением в крови лактата или с развитием уремии. Обычно присутствует небольшой кетоз вследствие голодания, поэтому также возможна кетонурия. [3]
Увеличение уровня лактата может свидетельствовать о тканевой гипоксии вследствие обезвоживания и, соответственно, сниженной перфузии. Сообщалось о резком повышении креатинфосфокиназы у больных с ГОК вследствие осложнения, связанного с рабдомиолизом [12].
Высокий уровень лактата также может указывать на сепсис [13].
Ввиду высокой частоты предшествующих хронических заболеваний необходим тщательный поиск провоцирующих факторов. Для этого проводятся общий анализ мочи, рентгенография грудной клетки, ЭКГ, посевы крови, мочи и мокроты. В связи с частым присутствием лихорадки и неврологических симптомов, включающих ригидность мышц затылка, может потребоваться спинномозговая пункция для исключения менингита [3].
Основные клинические характеристики
Типичная гиперосмолярная кома развивается, как правило, постепенно. Нарастают жажда, полиурия, слабость, может быть повышенный аппетит. На фоне постепенно нарастающего обезвоживания появляются психоневрологические и сердечно-сосудистые расстройства, т.е. гиперосмолярность проявляет себя преимущественно церебральным или кардиальным вариантом комы, что во многом зависит от предшествующего фона [7].
Специфических физических признаков, связанных с ГОК, не существует. Практически у всех больных имеет место значительная дегидратация. Обычные признаки дегидратации включают сухость слизистых оболочек, сморщенность языка, отсутствие потоотделения, западение и мягкость глазных яблок. Могут присутствовать постуральная гипотензия и рефлекторная тахикардия. У трети больных имеют место сосудистый коллапс и шок. Шок особенно часто наблюдается в присутствии грамотрицательной пневмонии. У трети больных отмечается также повышение температуры [3].
Такие симптомы, как жажда, полидипсия и полиурия, присущи как ДКА, так и гиперосмолярной коме, поскольку обусловлены одними и теми же патогенетическими механизмами – гипергликемией и осмотическим диурезом. Но их последствия при гиперосмолярной коме выражены значительно сильнее, поэтому и сердечно-сосудистые нарушения у этих больных более выражены. Отчасти это обусловлено и возрастом большинства больных ГОК, поскольку у пожилых больных уже до развития комы нередко имеется сердечная недостаточность. По этой же причине, т.е. из-за предшествовавшего снижения функции почек, у больных с гиперосмолярной комой чаще и раньше развивается олигурия и азотемия [2].
Характер дыхания вариабелен. Дыхание Куссмауля нехарактерно для неосложненной ГОК, однако гипервентиляция может присутствовать при наличии ацидоза другого генеза. Обычно наблюдается поверхностное дыхание при его учащении и одышке. Запах ацетона изо рта нехарактерен [3].
Наиболее выражены неврологические признаки. Особенность клиники ГОК – полиморфная неврологическая симптоматика, которая не укладывается в какой-либо четкий синдром, изменчива и исчезает при нормализации осмолярности. Практически у всех больных отмечается некоторое расстройство мышления: от неточных ответов на вопросы до спутанности сознания, сонливости, ступора и комы. Заторможенность больных прямо пропорциональна осмолярности крови. Средняя осмолярность у коматозных больных с ГОК составляет 380 мОсм/л. Угнетение сознания не коррелирует с концентрацией глюкозы, плазменным рН или параметрами СМЖ [3].
Однако не у всех больных с гиперосмолярным синдромом (ГС) развивается кома, поэтому следует с наибольшим вниманием отнестись к обследованию всех больных с ментальными нарушениями [3].
Из очаговых неврологических проявлений наиболее часто встречаются односторонние расстройства чувствительности и гемипарез. Примерно у 15 % больных отмечается судорожная активность, обычно очагово-моторного типа. Иногда возникают судороги по типу "grand mal". Могут наблюдаться тремор, мышечные подергивания, афазия, гиперрефлексия, мышечная слабость, угнетение глубоких сухожильных рефлексов, положительный симптом Бабинского, нистагм, гемианопсия, положительная плантарная реакция и ригидность мышц затылка. Иногда встречаются гемихореоатетоз или баллизм, бред или галлюцинации, приступы очаговой эпилепсии и паралич Тодда [3].
Патофизиологические механизмы, ведущие к ступору и коме, не совсем ясны. Возможно, здесь принимают участие несколько факторов. Было доказано, что осмолярность плазмы коррелирует с психическим состоянием. Большинство авторов сходится на том, что осмолярность – основной фактор, способствующий развитию ГОК. Другие возможные механизмы – ацидоз, нарушения мозгового кровообращения, диссеминированное внутрисосудистое свертывание, токсичность лизолецитина и СЖК, гипоксия и нарушения метаболизма углеводов в мозговой ткани [10].
Гиперосмолярность плазмы является движущей силой утечки воды из клеток мозга. Уменьшению объема клеток, следующему за их дегидратацией, препятствует медленная диффузия внутрь клетки осмотически активных веществ (напр., натрий или глюкоза), а также синтез «эндогенных осмолей». Это нераспознанные осмотически активные вещества, которые привносят свой вклад в осмотическое давление в клетках мозга, но не расцениваются как осмотически активные вещества. Считается, что они синтезируются из свободных аминокислот: глютамина, глютамата, аспартата. Очевидно, что подобные изменения внутриклеточных составляющих не могут не повлиять на клеточную возбудимость, что может сыграть свою роль в развитии энцефалопатии [10].
Также возможно, что гиперосмолярность разрывает гемато-энцефалический барьер, повреждая таким образом мозговую ткань и внося свой вклад в развитие энцефалопатии [10].
Осложнения
В ургентной терапевтической практике ГОК, как и различные варианты и степени выраженности ГС без потери сознания, привлекает к себе особое внимание в связи с высоким риском осложнений и в первую очередь различных коагулопатий: тромбоэмболий, ДВС-синдрома, а также отека мозга, обусловивших высокую летальность [7].
Пациенты с ГОК имеют повышенный риск артериальной и венозной тромбоэмболии. Исследования подтвердили, что пациенты с диабетом и гиперосмолярностью имеют повышенный риск развития венозных тромбозов наравне с пациентами с острой почечной недостаточностью, острым сепсисом, коллагенозами. Риск венозного тромбоза выше, чем у пациентов с кетоацидозом. Гипернатриемия и повышение уровня антидиуретического гормона усиливают тромбообразование путем изменений гемостатической функции и провоцирования гиперкоагуляции [13].
Лечение
Задачи лечения:
· Коррекция гиповолемии (восстановить потери жидкости и электролитов),
· Нормализовать осмолярность плазмы
· Нормализовать уровень глюкозы крови [13].
Другие мероприятия направлены на предотвращение:
· Артериальной и венозной тромбоэмболии
· Трофических язв нижних конечностей [13].
ГОК ассоциирована с более высокой смертностью, чем ДКА, и должна быть немедленно диагностирована и интенсивно лечиться. Потери жидкости оцениваются в пределах 100 – 220 мл/кг (10 – 22 л для пациента массой 100 кг). Определение объема регидратации должно основываться на оценке тяжести состояния пациента и наличия сопутствующих заболеваний. При лечении нужно соблюдать осторожность, особенно в отношении пожилых пациентов, у которых слишком быстрая регидратация может спровоцировать острую сердечную недостаточность, а недостаточная регидратация может привести к острому повреждению почек [13].
Пациенты с ГОК сложные и имеют сопутствующие заболевания, поэтому требуют тщательного наблюдения. Наличие хотя бы одного из нижеперечисленных параметров является показанием к помещению пациента в палату интенсивной терапии:
· Осмолярность плазмы более 350 мОсм/л
· Концентрация натрия более 160 ммоль/л
· pH венозной/артериальной крови менее 7,1
· Гипокалиемия (концентрация калия менее 3,5 ммоль/л) или гиперкалиемия (концентрация калия более 6 ммоль/л) при поступлении
· Менее 12 баллов по Шкале Комы Глазго
· Сатурация ниже 92 % (при учете отсутствия нарушений функции дыхания)
· Систолическое артериальное давление менее 90 мм рт. ст.
· Пульс более 100 или менее 60 ударов в минуту
· Диурез менее 0,5 мл/кг в час
· Креатинин плазмы более 200 ммоль/л
· Гипотермия
· Сосудистые нарушения, например инфаркт миокарда или инсульт
· Другие серьезные сопутствующие заболевания [13].
Осложнения в ходе лечения
Высокая летальность при ГОК обусловлена развитием осложнений, связанных как с самим патогенезом СД, так и с критическими состояниями, возникающими при нарушении углеводного обмена, а также с несвоевременностью и неадекватностью интенсивной терапии. В первую очередь это касается недостаточности контроля за адекватностью поддержания водно-электролитного баланса с развитием выраженной гипергидратации [1].
Массивное переливание гипотонического раствора способствует развитию отека мозга, хотя при ГОК это осложнение наблюдается реже, чем при ДКА [2].
Некоторые авторы, однако, оспаривают возможность развития отека мозга в ходе лечения ГОК. Несмотря на существующее равновесие между осмолярностью плазмы и СМЖ, составляющие их различны. Уровень глюкозы выше в плазме, в то время как уровень натрия значительно выше в СМЖ. У пациентов, умерших от ГОК, на вскрытии не было найдено морфологических изменений, характерных для отека мозга. Очевидно, несмотря на то, что уровень глюкозы в СМЖ снижается медленнее, чем в плазме, нарушения осмотического баланса между этими двумя жидкостями не происходит [11].
Следует помнить еще об одном осложнении массивной внутривенной инфузии гипотонических растворов – внутрисосудистом гемолизе, поэтому не рекомендуется использовать раствор хлорида натрия концентрацией меньше 0,45% [2]
У больных с выраженной недостаточностью функции почек (повышение содержания мочевины, остаточного азота и креатинина в сыворотке крови) инфузия жидкости с повышенной скоростью приводит к отеку легких [2].
Многие авторы отмечали ухудшение легочного газообмена при интенсивной терапии ГОК. В определенной мере эти изменения связаны с инфузионной терапией и носят ятрогенный характер. Они объясняли это развитием интерстициального отека легких в процессе регидратации. Патогенез развития отека легких связан с тремя этиологическими моментами: 1) увеличением внутрисосудистого гидростатического давления, 2) снижением КОД плазмы, 3) увеличением проницаемости сосудистой стенки. При проведении регидратации у больных действительно возникали все перечисленные факторы риска. Однако развития интерстициального отека легких не наблюдалось. Это может быть обусловлено тем, что при переливании большого объема кристаллоидных растворов срабатывает защитный механизм – значительно увеличивается легочный лимфоток и поток белка с ним, возвращаемый в сосудистое русло. Однако эффективность лимфотока значительно ограничивается сосудистой проницаемостью. Также было доказано, что на этапе регидратации развитие гипоксемии теснее связано с увеличением шунтирования крови в легких, чем с накоплением в них внесосудистой воды. Но все же полученные данные не могут исключать значения изменений транскапиллярного обмена жидкости в нарушениях легочного газообмена при проведении регидратации [1].
Некоторые авторы утверждают, что лечение ГОК также может усугубить течение ишемического инсульта, развившегося вследствие ГОК. Несколько возможных патофизиологических механизмов процессов могут объяснить непредвиденно высокий риск развития этого осложнения после лечения ГОК. Во-первых, ухудшенный метаболический профиль у пациентов с ГОК может частично объяснить увеличение числа инсультов. Вторая теория связывает развитие ГОК у пациентов с СД со значительными колебаниями уровня глюкозы. Перемежающая гипергликемия может индуцировать дисфункцию эндотелиальных клеток и ассоциирована с окислительным стрессом. Другие исследования показали, что колебания уровня глюкозы могут вызвать пролиферацию клеток, высвобождение цитокинов и нарушение функции эндотелия – все это приводит к острому нарушению мозгового кровообращения (ОНМК) [14].
Arieff и Carroll в своих исследованиях указывают на развитие таких осложнений после терапии ГОК, как сосудистый коллапс и острый тубулярный некроз (ОТН). Высокая концентрация глюкозы во внеклеточной жидкости защищает это водное пространство от гиповолемии за счет внутриклеточных запасов воды. В случае быстрого снижения концентрации глюкозы при введении больших доз инсулина недостаточное осмотическое давление во внеклеточной жидкости может вызвать перемещение большого объема воды внутрь клетки, что приведет к гиповолемии и сосудистому коллапсу. Подобным образом обусловленный гипергликемией осмотический диурез защищает почки от ОТН на фоне сниженной почечной перфузии. В случае быстрого снижения уровня глюкозы осмотический диурез уменьшается, что может привести к развитию ОТН [3, 11].
Таблица 1. Осложнения, возникающие при ДКА и ГГС (гипергликемическом синдроме) в ходе их лечения [8].
|
Осложнение |
Причины, способствующие факторы или условия возникновения |
|
Гипогликемия |
· Введение избыточной дозы инсулина, в т.ч. применение режима «больших доз» · Недостаточно частый контроль гликемии · Несоблюдение критериев начала инфузии 5% глюкозы в ходе терапии · Позднее начало перорального питания пациента, недостаточное количество углеводов в пище |
|
Гипокалиемия |
· Начало инсулинотерапии при низком уровне калия в сыворотке · Недостаточный мониторинг уровня калия · Позднее начало и несоблюдение скорости инфузии калия при нормо- и гипокалиемии · Коррекция ацидоза большими дозами бикарбоната натрия или трисамина |
|
Отек легких, РДСВ |
Перегрузка жидкостью (избыточный объем инфузии), слишком быстрое снижение гликемии и осмолярности плазмы (введение избыточных доз инсулина или избыточного объема гипотонического раствора натрия хлорида, недостаточно частое определение осмолярности) |
|
Отек мозга |
· Возможен при нелеченом кетоацидозе · Слишком быстрое снижение гликемии и/или осмолярности плазмы (введение избыточных доз инсулина или избыточного объема гипотонического раствора натрия хлорида, недостаточно частое определение осмолярности) · Избыточное введение бикарбоната натрия |
|
Гиперхлоремический ацидоз |
Перегрузка раствором натрия хлорида |
|
Рабдомиолиз |
Возможно, катаболизм белка как следствие инсулиновой недостаточности |
|
Острые артериальные и венозные тромбозы и тромбоэмболии |
Дегидратация, повышение вязкости крови и гематокрита, усиление свертываемости, характерные для нелеченого кетоацидоза и гиперосмолярного состояния |
Библиографическая ссылка
Концедайло П.Е. ГИПЕРОСМОЛЯРНАЯ КОМА: ПРЕДРАСПОЛАГАЮЩИЕ ФАКТОРЫ, ОСМОЛЯРНОСТЬ ПЛАЗМЫ КРОВИ, ПАТОГЕНЕЗ, ЛАБОРАТОРНЫЕ ПОКАЗАТЕЛИ, ОСНОВНЫЕ КЛИНИЧЕСКИЕ ХАРАКТЕРИСТИКИ, ОСЛОЖНЕНИЯ, ЛЕЧЕНИЕ, ОСЛОЖНЕНИЯ В ХОДЕ ЛЕЧЕНИЯ. // Международный студенческий научный вестник. – 2016. – № 2. ;URL: https://eduherald.ru/ru/article/view?id=14341 (дата обращения: 23.04.2024).

